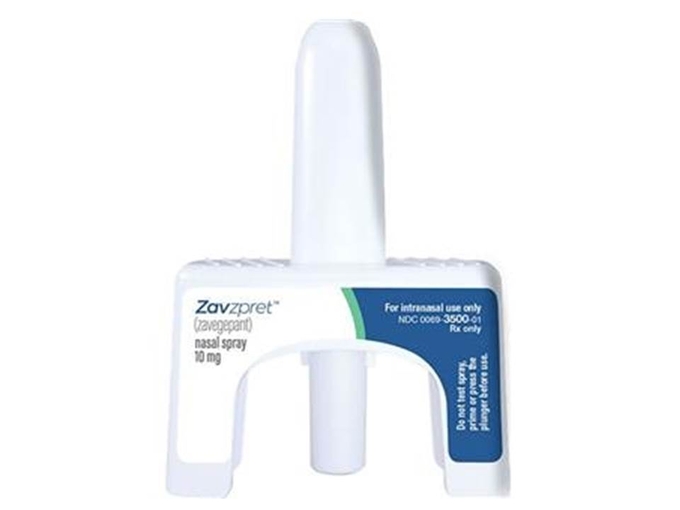
비강 분무형 자베게판트인 자브즈프렛(Zavzpret)이 급성 편두통 치료제로 미국 식품의약국(FDA)의 승인을 받았다고 의학 뉴스 포털 메드페이지 투데이(MedPage Today)가 화이자 제약회사의 발표를 인용, 최근 보도했다.
FDA는 칼시토닌 유전자 관련 펩티드(CGRP) 수용체 길항제인 자베게판트 비강 스프레이를 급성 편두통 치료제로 최초 승인했다고 화이자사는 밝혔다.
화이자사는 바이오헤이븐(Biohaven) 제약회사로부터 인수한 비강 스프레이 형 자베게판트에 자브즈프렛이라는 새로운 브랜드 이름을 붙여 오는 7월 출시할 예정이다.
자브즈프렛은 전조 증상이 있거나 없는 편두통에 효과가 있으며 편두통 예방약은 아니다.
편두통은 병리생리학적으로 CGRP 경로와 연관이 있다. 그래서 경구 또는 주사형 CGRP 억제제들이 지난 몇 년 사이에 FDA의 승인을 받았다.
비강 스프레이 형 CGRP 억제제가 승인된 것은 이번이 처음이다.
FDA의 자브즈프렛 승인은 두 차례에 걸친 3상 임상시험 결과에 근거한 것이다.
3상 임상에서 자브즈프렛이 투여된 그룹은 투약 15분 후 15.9%가, 위약이 투여된 대조군은 8%가 급성 편두통이 사라졌다.
투약 30분 후에는 자브즈프렛 그룹은 30.5%, 대조군은 20.3%가 편두통이 진정됐다.
대조군보다 빈도가 높게 나타난 자브즈프렛의 부작용은 무미각증(ageusia), 미각 이상증(dysgeusia) 같은 미각 장애, 오심, 구토, 비강 불편 등이었다.
자베게판트는 금기사항이 있다. 자베게판트 또는 자베게판트에 함유된 성분에 대해 과민반응(얼굴 부종, 두드러기 등)을 겪은 일이 있는 사람은 사용하지 말아야 한다.